

细胞通过哺乳动物雷帕霉素靶蛋白复合物1(mTORC1)信号通路感知营养物质如氨基酸(AAs)进而调控生长与代谢,是一种生物进化过程中高度保守的生存适应方式。在肿瘤微环境(TME)中,尽管普遍存在营养不足,但癌细胞mTORC1信号为何异常激活这一现象与肿瘤进展过程中的免疫逃逸有何关系这些科学问题引起该团队的极大兴趣。
该团队经过数年攻关,发现TME多种炎症因子(如TNFα、IFNγ等)通过诱导ZBTB5蛋白S127残基磷酸化,“劫持”癌细胞的固有氨基酸感应系统,驱动mTORC1异常激活,促进肿瘤细胞大量摄取氨基酸,引发CD8+T细胞因营养饥饿而凋亡,导致免疫逃逸、肿瘤发生和免疫耐药。这个过程中ZBTB5-pS127发挥炎症感应器的关键功能,针对该靶点设计特异性阻断肽,在多种模型中抑制肿瘤进展,有效逆转耐药、大幅增敏免疫治疗。
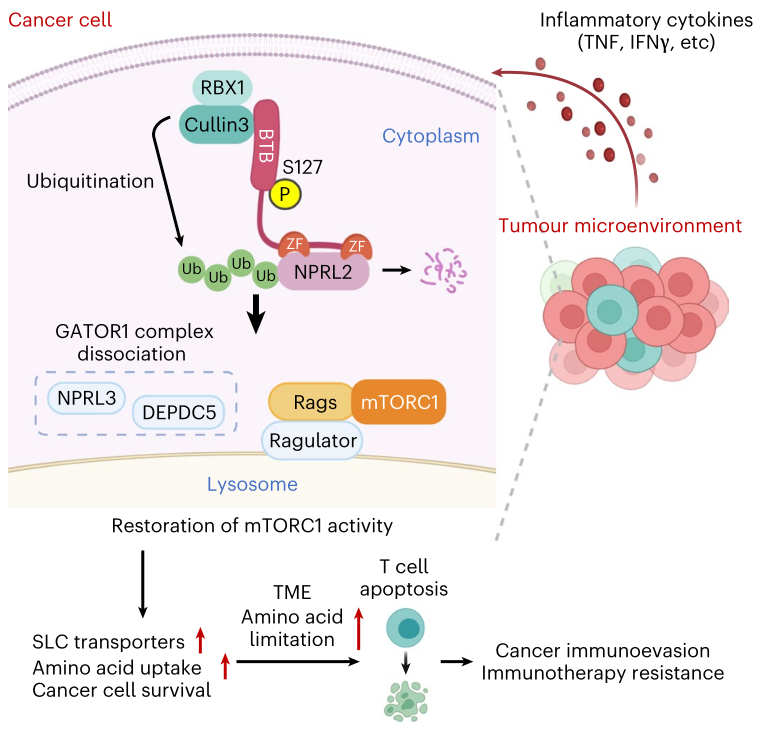 ▲异常氨基酸感应通过炎性细胞因子-ZBTB5-mTORC1轴促进免疫治疗耐药性
▲异常氨基酸感应通过炎性细胞因子-ZBTB5-mTORC1轴促进免疫治疗耐药性
该团队分析胃癌等多种炎性相关恶性肿瘤,发现TME炎症状态与癌细胞mTORC1活性密切相关。为严谨地模拟TME营养状态,团队自主开发了一种肿瘤间质液AAs浓度类似的培养体系,发现在炎症因子刺激通过JNK/p38激酶,磷酸化ZBTB5蛋白的Ser127位点(ZBTB5-pS127)。这一磷酸化事件促进Cullin3ZBTB5E3泛素连接酶复合物的组装,该复合物特异性催化NPRL2蛋白发生K48多聚泛素化修饰,并通过蛋白酶体途径降解,进而破坏GATOR1复合物完整性。由于GATOR1复合物是mTORC1营养感知信号通路的关键抑制因子,通过上述方式癌细胞在营养匮乏TME中保持mTORC1高度激活。因此,这条全新的细胞信号转导通路代表了炎症信号“劫持”营养感应通路的核心分子路径。
在肿瘤生物学功能方面,团队发现ZBTB5-pS127-mTORC1轴对癌细胞增殖作用较小,主要通过上调多种SLC家族转运蛋白(如SLC6A14、SLC43A2),显著增强癌细胞对氨基酸(包括甲硫氨酸、谷氨酰胺等)的摄取能力,从而大幅降低肿瘤间质液中的氨基酸水平。这种营养剥夺导致浸润的CD8⁺T细胞因“饥饿”而发生凋亡,进而抑制抗肿瘤免疫、实现免疫逃逸。在多种免疫治疗的临床肿瘤样本中,这条信号轴激活与CD8⁺T细胞浸润减少、抗PD-1治疗反应差及不良预后密切相关。在靶向干预方面,封闭ZBTB5-pS127位点可特异性阻断Cullin3ZBTB5复合物形成,上调TME氨基酸水平,恢复CD8⁺T细胞活性,在多种小鼠模型中显著抑制肿瘤生长、延长生存期,逆转免疫治疗的原发性和获得性耐药。这些发现为改善肿瘤免疫治疗,尤其对于耐药患者带来新的契机。
《Nature Cell Biology》由Nature Portfolio主办,刊载细胞生物学及相关领域具有重大科学突破和应用潜力的研究、综述和评论,为细胞生物学家、分子生物学家及医学研究者提供前沿学术参考和机制洞见。2024年影响因子19.1,JCR分区Q1。
点击下方阅读原文,访问原文链接。