


结直肠癌(colorectal cancer,CRC)是全球高发的恶性肿瘤之一。目前,以手术、放化疗及联合治疗为主的传统策略对转移性患者疗效有限,而新兴的免疫疗法也仅能使少数患者获益。因此,探索新的治疗靶点,改善患者预后,已成为领域内亟待解决的关键问题。CRC的发生发展涉及基因突变累积、代谢重编程、表观遗传改变及肿瘤微环境重塑等多个层面。其中,代谢重编程作为实体肿瘤的重要特征,在临床相关性及靶向药物开发方面均展现出巨大潜力,尤其是脂质代谢重编程备受关注。然而,作为多种脂质的合成骨架,脂肪酸的代谢重编程在CRC进展中的作用尚不明确,其是否影响肿瘤微环境以及具体机制如何,尚未阐明。
研究团队首先通过分析多组转录组测序数据,结合临床信息,筛选出与CRC脂肪酸重编程密切相关的关键酶——ACADS。随后,在免疫健全小鼠、裸鼠及条件性敲除鼠中构建多种CRC模型,结合单细胞测序、多重免疫荧光及流式细胞术等技术,证实ACADS通过重塑肿瘤免疫微环境发挥抑瘤功能。为进一步明确机制,团队通过测序及细胞、动物水平的干预实验,揭示mtDNA介导的cGAS-STING信号通路是ACADS发挥抑瘤作用的关键环节。深入排查后发现,ACADS缺失导致的mtDNA遗漏减少,与其自身的修饰密切相关。借助质谱分析、免疫共沉淀及超分辨显微镜等技术,研究证实ACADS与mito-DNMT1存在相互作用,并影响mtDNA的甲基化水平。干预mito-DNMT1的表达,可重现ACADS相关的表型,进一步验证了该调控轴的关键作用。
为验证ACADS-mito-DNMT1-cGAS-STING信号通路的临床相关性,团队收集了77例结直肠癌患者样本进行分析,结果显示该信号通路与CRC的恶性进展密切相关。最后,团队通过虚拟筛选鉴定出金丝桃素(Hypericin)作为ACADS的激活剂。功能实验表明,金丝桃素发挥抑瘤作用具有ACADS依赖性,进一步证实了ACADS作为潜在治疗靶点的可行性。
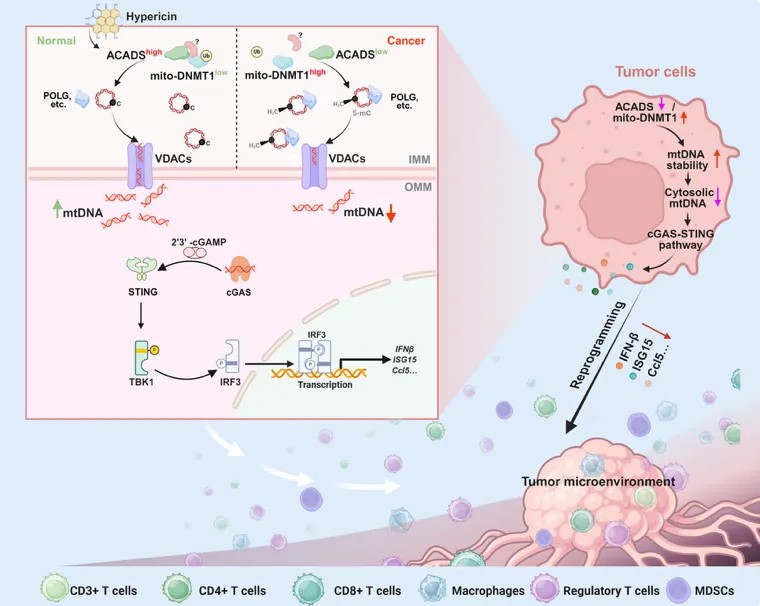
▲ACADS通过调控线粒体DNA甲基化激活抗肿瘤免疫机制
综上所述,该研究揭示了脂肪酸代谢重编程促进结直肠癌免疫逃逸的新机制,并筛选出靶向激活ACADS-mito-DNMT1-cGAS-STING通路的天然小分子化合物金丝桃素。值得注意的是,金丝桃素在其他肿瘤中已进入III期临床试验,具有良好的临床转化基础。这一发现为基于ACADS的结直肠癌靶向治疗策略提供了有力的理论依据和潜在的候选药物,具有重要的科学意义与临床前景。
《Signal Transduction and Targeted Therapy》由Springer Nature出版,刊载与生理和病理过程中信号转导的各个方面有关的原创研究文章和评论文章,以及用于治疗人类疾病(如癌症、自身免疫性疾病等)的生物制剂和小分子药物形式的信号转导靶向治疗。2025年影响因子52.7,JCR分区Q1。
点击下方阅读原文,访问原文链接。