

以 PD-1/PD-L1 为代表的免疫检查点抑制剂已显著改变恶性肿瘤治疗格局,但其临床应用仍面临响应率有限、免疫相关不良反应频发、耐药机制复杂等关键问题。肿瘤微环境中髓系细胞的 PD-L1 表达是调控抗肿瘤 T 细胞免疫应答的核心节点。然而,驱动肿瘤微环境内髓系细胞 PD-L1 表达的上游分泌型调控因子、特异性受体及下游信号通路尚未被系统阐明。人附睾蛋白 4(HE4)是一种在肺腺癌、卵巢癌等多种肿瘤中异常高表达的分泌型糖蛋白,作为临床常用肿瘤标志物,其在肿瘤免疫微环境重塑及免疫逃逸中的作用与分子机制仍不明确。基于此,本研究旨在揭示 HE4 调控髓系细胞 PD-L1 的具体机制,明确其在肿瘤免疫逃逸中的功能,并探索其作为免疫治疗靶点与疗效预测标志物的转化价值。
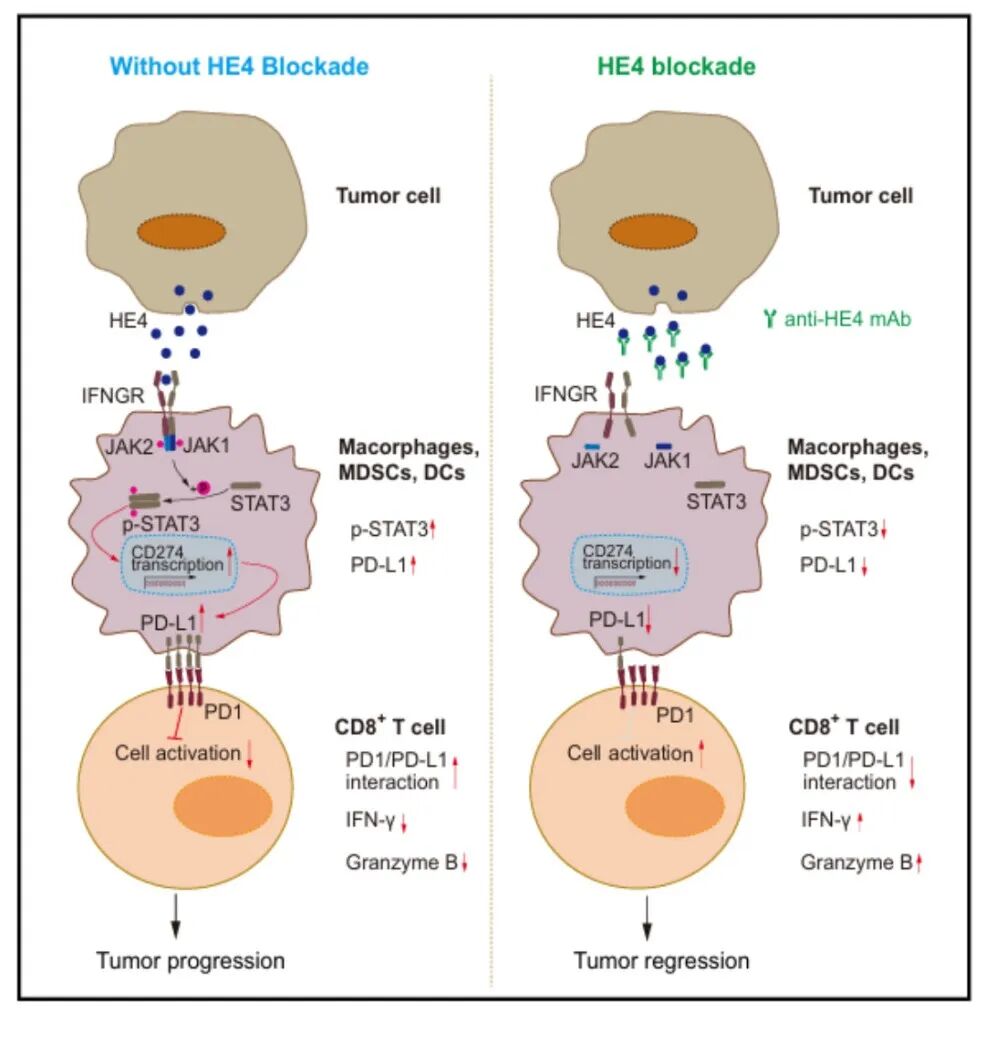 ▲HE4调控髓系PD-L1介导肿瘤免疫逃逸的机制
▲HE4调控髓系PD-L1介导肿瘤免疫逃逸的机制
本研究通过临床样本分析、动物模型、分子生化实验及单细胞测序等手段展开系统研究。结果显示,HE4 在肺腺癌及卵巢癌肿瘤组织中显著高表达,其促肿瘤进展作用不依赖对肿瘤细胞的直接调控,而是通过适应性免疫途径来实现。机制上,肿瘤分泌的 HE4 可直接结合髓系细胞表面 IFN-γR1/2 受体,选择性激活 JAK-STAT3 信号通路,在转录水平上调 PD-L1 表达,该过程不依赖 IFN-γ、STAT1 及NF-κB 等经典通路;同时,肿瘤微环境中 HE4 浓度远高于 IFN-γ,可通过浓度优势竞争性结合 IFN-γR,抑制 IFN-γ-STAT1 通路活化,降低其促炎与抗肿瘤效应,重编程髓系细胞向免疫抑制表型转化。功能实验证实,HE4 敲除或中和抗体阻断可显著降低巨噬细胞、树突状细胞及髓源抑制细胞的 PD-L1 水平,恢复CD8+T细胞的活化与效应功能,在肺癌、卵巢癌等多种小鼠模型中有效抑制肿瘤生长,且可与抗 CTLA-4 免疫治疗、紫杉醇化疗产生协同增效作用。安全性评价表明,抗 HE4 治疗引发的炎症因子释放、多器官免疫炎症及肝肾功能损伤发生率显著低于 PD-1 抑制剂,具备更优的治疗安全窗。临床队列验证显示,肺腺癌组织中高 HE4 表达与 PD-1 抑制剂治疗良好响应显著相关,其预测效能优于传统 PD-L1 标志物。
本研究首次揭示 HE4-IFN-γR-JAK-STAT3-PD-L1 是调控髓系免疫抑制及肿瘤免疫逃逸的全新分子轴,明确了 HE4 作为肿瘤源性分泌蛋白调控肿瘤免疫微环境的关键机制,完善了 PD-L1 的转录调控网络。研究结果证实 HE4 兼具肿瘤免疫治疗靶点与 PD-1/PD-L1 疗效预测标志物的双重价值,为开发更安全、高效的肿瘤精准免疫治疗策略提供了新的理论依据与重要转化方向。
《Cell Reports Medicine》由Cell Press出版,刊载前沿的转化和临床生物医学科学研究,为人类健康和医学提供信息和影响。
点击下方阅读原文,访问原文链接。