
近日,陆军军医大学西南医院、金凤实验室卞修武院士和平轶芳教授团队合作,在国际期刊Science Advances(中科院大类一区TOP期刊,影响因子:12.5)上发表了题为“FAM50A drives breast cancer brain metastasis through interaction with C9ORF78 to enhance ʟ-asparagine production”的研究性论文。

原发乳腺癌因治疗手段的进步,已经获得了较好的5年生存期。然而,转移的发生却给患者的生存带来了极大挑战。尽管现代医学在靶向治疗和免疫疗法方面取得了显著进展,但转移性病灶的控制仍然是一个艰巨的任务。
骨、肺、肝和脑是乳腺癌四个常见的转移部位。乳腺癌脑转移(BCBM)占所有转移性乳腺癌病例的10–30%,与不良预后相关,并损害患者的认知和感官功能,导致生活质量严重受限(1)。针对BCBM患者目前可用的治疗方式包括手术、全脑放射治疗、立体定向放射外科以及化疗,或这些疗法的联合使用。然而,由于血脑屏障限制了药物渗透性,且存在化疗耐药性,BCBM患者的预期寿命仍然不尽如人意(2)。因此,阐明BCBM的分子机制以寻找新的治疗靶点、提高治疗效果并改善BCBM患者预后刻不容缓。
该研究发现并鉴定了调控乳腺癌脑转移的关键分子——FAM50A,多重的实验证据表明,FAM50A促进了乳腺癌脑转移的发生,而敲除它能够明显抑制脑转移的发生,使得模型小鼠获得更好的无脑转移生存。进一步的研究揭示了它的作用机制:FAM50A通过与C9ORF78相互作用,促进了下游分子ASNS的表达。而后者是天冬酰胺合成酶,促进了乳腺肿瘤细胞内天冬酰胺水平的增高,而这又进一步增强了其脑转移能力。转化意义上,本研究发现一种原本用于治疗白血病的药物——天冬酰胺酶,通过降低小鼠体内的天冬酰胺水平,显著抑制了乳腺癌脑转移的发生。本研究证实,乳腺癌脑转移依赖于高水平的天冬酰胺,填补了乳腺癌脑转移领域氨基酸依赖性研究方向上的空白。
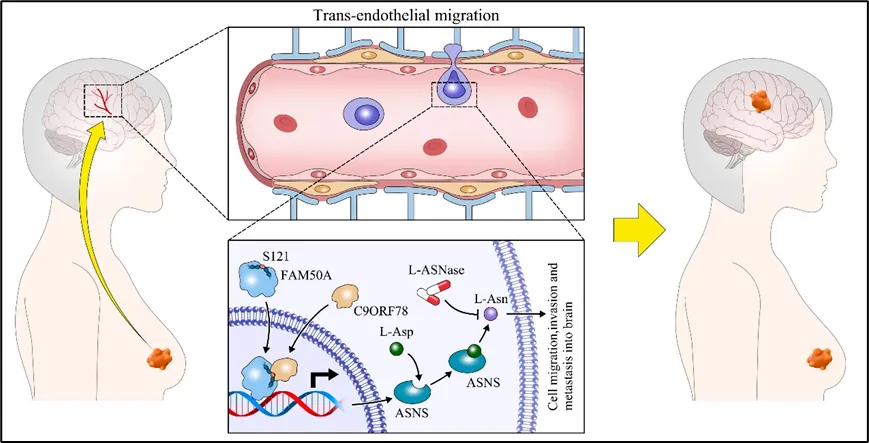
▲本研究工作的机制示意图。FAM50A-C9ORF78-ASNS信号通路是乳腺癌脑转移的新型治疗靶点,靶向该通路或者使用天冬酰胺酶具有抑制脑转移的应用潜力,为乳腺癌患者脑转移的预防、控制提供新思路。
参考文献:
1. Kanchan RK, Siddiqui JA, Mahapatra S, Batra SK, and Nasser MW. microRNAs Orchestrate Pathophysiology of Breast Cancer Brain Metastasis: Advances in Therapy. Mol Cancer. 2020;19(1):29.
2. Wang Y, Ye F, Liang Y, and Yang Q. Breast cancer brain metastasis: insight into molecular mechanisms and therapeutic strategies. Br J Cancer. 2021;125(8):1056-67.
《Science Advances》由美国科学促进会(AMER ASSOC ADVANCEMENT SCIENCE)出版,是聚焦多学科领域的开放获取期刊,涵盖各学科及跨学科研究方向,内容兼顾学科内深度研究与跨学科创新成果(如各领域有影响力的研究论文和综述)。期刊2025年最新影响因子为12.5,在JCR分区中为Q1区,中科院2025年3月升级版大类及小类学科「综合性期刊」均位于1区,且为Top期刊,是全球科研人员发表有影响力研究成果的重要平台。
点击左下方阅读原文,访问原文链接。
https://pubs.acs.org/doi/10.1021/acsnano.5c02492