科研进展
卞修武院士团队研发新型MOF基纳米药物增强三阴性乳腺癌放疗效果
放射治疗(RT)是局部控制三阴性乳腺癌症(TNBC)的重要临床治疗方法之一,但放射耐药性仍然限制着这一策略的治疗效果。鉴于此,陆军军医大学西南医院、金凤实验室卞修武院士、仰毅教授和田甘教授团队以双重放射增敏方式设计了一种ATP/pH双响应释放MOF基纳米药物,可有效递送铁离子并抑制谷胱甘肽(GSH)的合成从而协同诱导铁死亡,结合高原子序数纳米材料的放疗增敏效应,共同促进了TNBC的放射治疗效果。该研究以题为“A MOF-based Potent Ferroptosis Inducer for Enhanced Radiotherapy of Triple Negative Breast Cancer”的论著形式发表在《ACS Nano》上。

该纳米材料合成过程如图1所示。首先通过一步法将L-丁硫氨酸-亚砜亚胺(BSO)负载于ZIF-8内,然后在其表面生长金纳米粒子(Au
NPs)。以BSO/ZIF-8@Au为模板,生长铁基金属多酚(MPN)网络结构,最后修饰透明质酸(HA)获得最终纳米材料BSO/ZIF-8@Au@MPN@HA
(BZAMH)。BSO可抑制γ-谷氨酰半胱氨酸合成酶(γ-GCS),减少胞内GSH的生物合成,从而间接灭活GPX4。MPN释放的Fe2+可通过芬顿效应产生羟基自由基(•OH)。GPX4的失活和局部生成•OH共同诱导强效铁死亡。修饰后的Au NPs可改善入射X射线的能量沉积。各组分协同促进铁死亡并增强RT以有效治疗TNBC,同时抑制TNBC肺转移(图1B)。
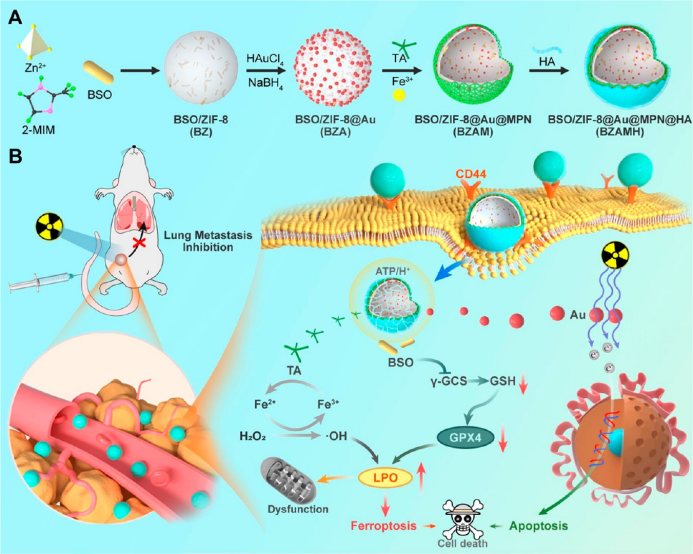
▲图1. MOFs基铁死亡纳米诱导剂的合成路线及作用机理图
【BZAMH NPs的物理化学性质表征】
所制备的BZAMH NPs呈现空心球状结构,水合粒径约为200nm。当生长了MPN壳层之后,由于TA的刻蚀与还原作用,BZAMH NPs转化为非晶态空心结构,并且表面的铁离子以Fe2+居多,为后续的芬顿反应提供了有利条件。
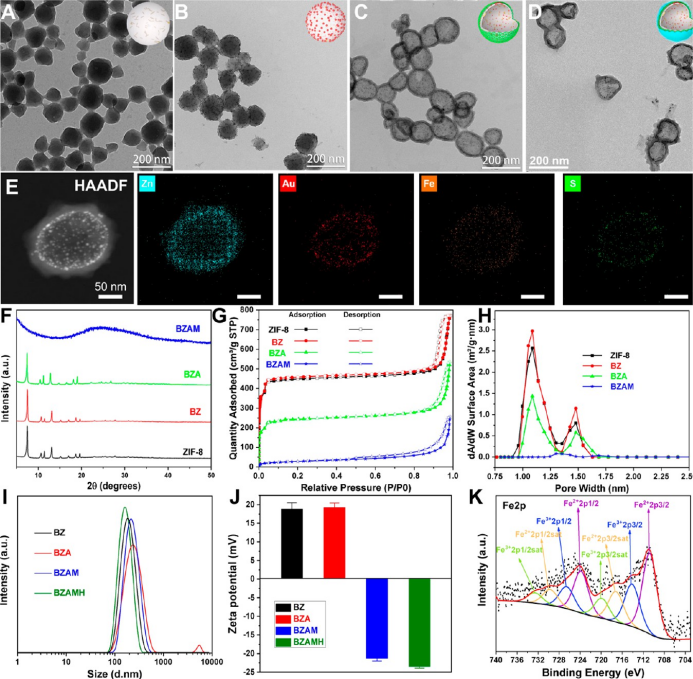
▲图2. BZAMH NPs的物理化学性质表征
【BZAMH NPs可有效诱导铁死亡】
BZAMH NPs消耗细胞GSH和放大氧化应激诱导铁死亡。实验以4T1小鼠细胞为模型,证明了BZAMH NPs可被细胞有效内吞,并能成功消耗细胞内的GSH,下调GPX4表达,造成脂质过氧化物(LPO)的累积,从而诱导明显的铁死亡效应。
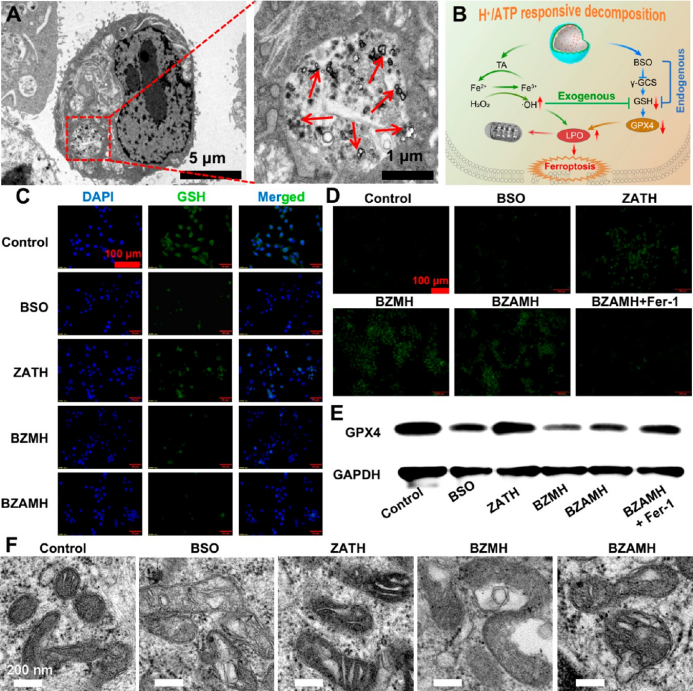
▲图3. BZAMH NPs可有效诱导铁死亡
【铁死亡可与Au NPs协同增强RT】
铁死亡可增强RT,并与Au介导的放射增敏作用协同。实验证明了铁死亡和Au NPs都可以明显促进RT对肿瘤细胞的抑制作用,BZAMH NPs可以协同两者的作用,造成更明显的DNA损伤,表现出最强的细胞生长抑制作用。
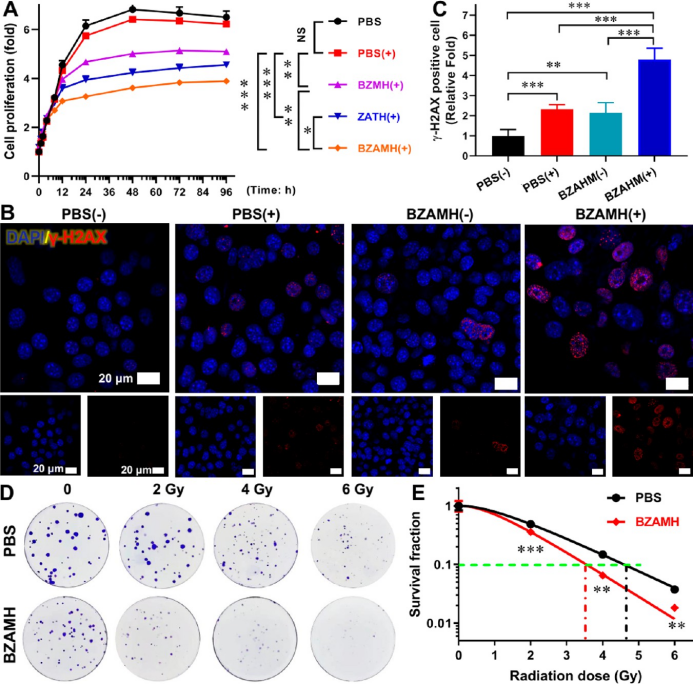
▲图4. 铁死亡可与Au NPs协同增强RT
【体内抗肿瘤实验】
BZAMH NPs在体内表现出明显的肿瘤生长抑制作用。基于体外治疗的研究结果,我们进一步研究了BZAMH
NPs在体内的抗肿瘤作用。实验表明,BZAMH+X-ray介导的铁死亡和RT具有最明显的肿瘤生长抑制效果,延长了小鼠的生存期。对肿瘤组织进行切片染色发现,BZAMH+X-ray可以显著降低Ki67和GPX4的表达,造成严重的DNA损伤,从而成功抑制细胞增殖和肿瘤生长。
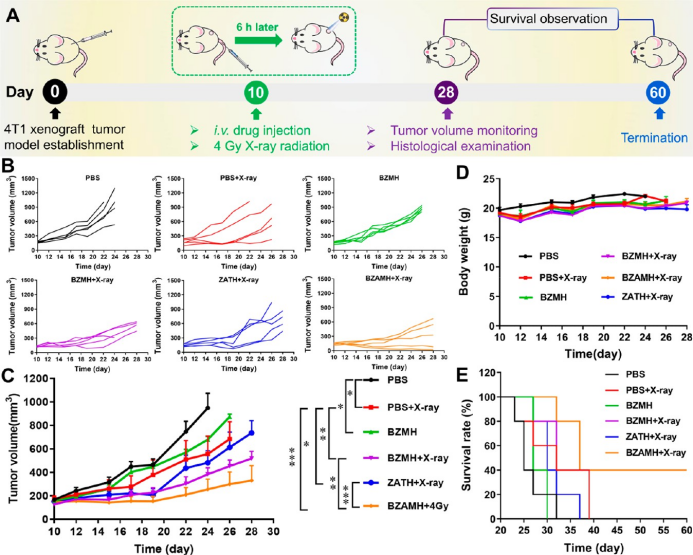
▲图5. BZAMH NPs体内抗肿瘤实验
【抗肺转移研究】
采用血流转移和乳腺癌原位肺转移双模型研究了BZAMH
NPs的抗转移能力。血流模型研究发现,BZAMH+X-ray可以明显抑制小鼠肺部肿瘤结节的产生;乳腺癌原位肺转移模型研究发现,BZAMH+X-ray不仅可以抑制原位肿瘤的生长,同样可以减少乳腺癌肺转移的情况发生。
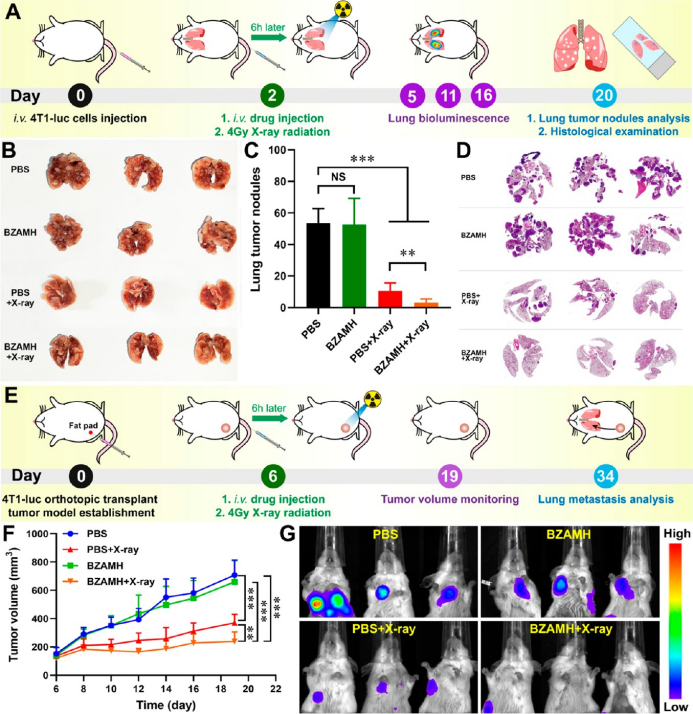
▲图6. 抗肺转移研究
【小 结】
该研究开发了一种MOFs基纳米药物,可控递送亚铁离子以引发类芬顿效应以执行铁死亡,且可抑制GSH生成使得GPX4失活以破坏铁死亡防御系统,二者协同诱导强烈的铁死亡。结合Au NPs的放疗增敏效应,高效抑制肿瘤的生长同时表现出更强的抗乳腺癌肺转移疗效。总之,本研究引入的智能纳米药物为抗癌治疗提供了新的见解,有望为下一代纳米药物的发展提供可靠的参考。
|
 2023年6月6日
2023年6月6日

